Lægemiddelinteraktioner
Rationel farmakoterapi nr. 6, 2015
Vær opmærksom på, at Rationel Farmakoterapi 2, 2020 også indeholder information om lægemiddelinteraktioner i almen praksis: Lægemiddelinteraktioner i almen praksis
Af Kenneth Skov og Torben Laursen
Enheden for Lægemiddelovervågning og Medicinsk Udstyr, Sundhedsstyrelsen.
Klinisk Farmakologisk afdeling, Aarhus Universitetshospital
Lægemiddelinteraktioner er et allestedsnærværende problem i sundhedsvæsenet. De fleste læger kender formentlig til de væsentligste interaktioner inden for deres eget speciale, men især hos patienter i polyfarmaci kan problemet være svært at overskue. Heldigvis findes der flere værktøjer til beslutningsstøtte, men viden om korrekt brug og begrænsninger er en forudsætning for, at de kan anvendes klinisk. I denne artikel vil vi give en basal introduktion til interaktioner. Vi vil især præsentere Sundhedsstyrelsens Interaktionsdatabase, dennes opbygning og basis for klassificering af lægemiddelpåvirkninger. Herunder vil vi også kort berøre andre opslagsværker/databaser, da der kan være diskrepans mellem disse, i og med de ofte bygger på vurderinger af litteraturen. Vi vil ydermere give læseren et indblik i kommende tiltag på området.
Interaktioner
Alt efter på hvilket niveau to lægemidler interagerer tales om farmakodynamiske og farmakokinetiske interaktioner. Farmakodynamiske interaktioner relaterer til virkningen af lægemidlet og er hyppigt forekommende, men er ofte forudsigelige (fx virkning på samme receptor eller homeostase fx blodtryk, koagulation, blodsukker) og dermed en mindre udfordring i klinikken. Farmakokinetiske interaktioner er relateret til lægemidlets skæbne i kroppen og er sjældnere, men også langt mere uberegnelige og kan potentielt føre til svære bivirkninger eller behandlingssvigt.
Farmakodynamiske interaktioner
Farmakodynamiske interaktioner forekommer, når to (eller flere) lægemidler har indvirkning på samme receptor, målorgan eller fysiologiske system. De er enten additive, synergistiske eller antagonistiske. Farmakodynamiske interaktioner er ofte klinisk forudsigelige og bruges ofte rationelt i farmakoterapien − fx ved anvendelse af flere forskellige antihypertensiva til behandlingsresistent eller svær hypertension. Farmakodynamiske interaktioner, der giver betydelige bivirkninger, ses dog også. Fx ses flere blødninger − især gastrointestinalt − ved kombination af SSRI-præparater og NSAID end de to stofgrupper hver for sig. Inden for CNS/psykiatri-behandlingen kan kombinationer af psykotrope lægemidler som SSRI’er, ADHD-midler, antipsykotika, MAO-hæmmere og/eller tricykliske antidepressiva medføre øget risiko for serotonergt syndrom. Risikoen kan øges yderligere ved samtidig behandling med andre stoffer med indvirkning på det serotonerge system, fx tramadol eller triptaner.
Farmakokinetiske interaktioner
Farmakokinetiske interaktioner kan principielt forekomme på alle trin i et lægemiddels vej gennem organismen. Særligt ved aktiv transport over membraner, metabolisme eller udskillelse er lægemidlet tilgængeligt for påvirkninger. Det er især de små kemiske lægemiddelmolekyler, der interagerer. Dette skyldes, at de opfattes som fremmede af organismen. Biologiske og endogene lægemidler efterligner kroppens egne mekanismer og har derfor kun ringe interaktionspotentiale.
Langt de fleste små kemiske lægemidler metaboliseres i leveren. De kan i leveren undergå både fase I- og fase II-reaktioner. Ved fase I-reaktioner sker oxidering, hydroxylering eller reduktion. Ved fase II-reaktioner konjugeres eller glukuronideres læge-midlet. Herved skabes metabolitter, der er nemmere for kroppen at udskille.
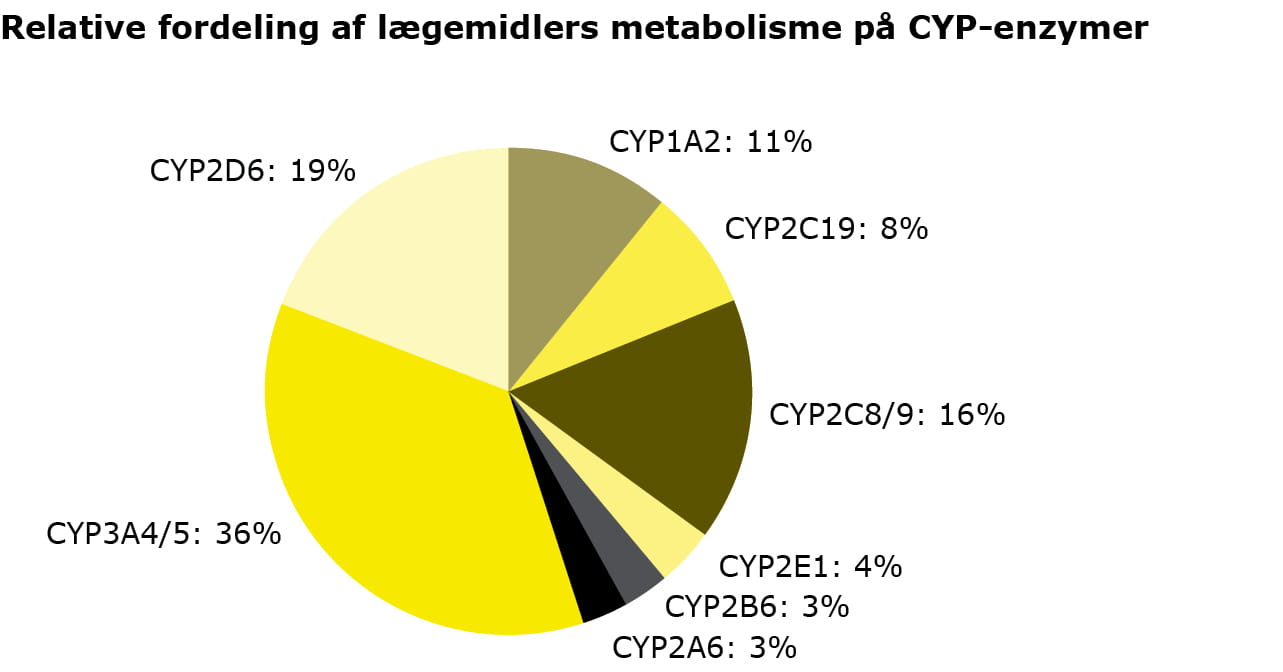
Fase I-reaktioner faciliteres primært af leverens cytokrom-P450(CYP) enzymsystem. CYP-systemet er evolutionært et værktøj for kroppen til at uskadeliggøre og udskille toksiner fra organismen. Disse enzymer er evolutionært udviklet i mange forskellige retninger for at modvirke skiftende udefra kommende trusler. Lægemidler skal i denne sammenhæng betragtes som toksiner for organismen. I forlængelse heraf kan lægemidler metaboliseres af forskellige og evt. flere CYP-enzymer. Figuren viser den relative fordeling af lægemidlers metabolisme på CYP-enzymer.
Det er et krav i lægemiddeludviklingen, at medicinalfirmaet undersøger lægemidlets metaboliske pathway og eventuelle ind-virkning på CYP-systemet. Så længe denne metabolisme ikke påvirkes, kan vi med nogen inter-individuel variation forudse lægemidlets skæbne i organismen.
Nogle lægemidler har evnen til at inducere eller inhibere disse enzymer. Situationen kompliceres yderligere af, at nogle lægemidler er afhængig af CYP-enzymer for at kunne metaboliseres til aktive metabolitter, fx clopido-grel, mens andre igen selv er aktive, men også har aktive metabolitter, fx kodein og tramadol.
De 4 A’er
De inhibitorer og inducere, der har størst betydning for klinikeren, kan groft inddeles i 4 grupper − de 4 A’er. Har man disse in mente, når man vurderer risiko for interaktioner, kan langt størstedelen af klinisk betydende farmakokinetiske interaktioner forudses. Se tekstboks.
Denne tommelfingerregel er naturligvis ikke udtømmende, men kan forebygge mange potentielle lægemiddelska-der/bivirkninger.
Farmakokinetiske interaktioner forekommer også på fase II-niveau. Om end disse interaktioner er sjældnere grundet den store kapacitet, kan lægemidler også både inhiberes og induceres på dette niveau. Fx øges halveringstiden af lamotrigin til næsten det dobbelte ved samtidig behandling med valproat − grundet inhibition af enzymet uridindifosfat-glukuronosyltransferase. Således skal lamotrigindosis reduceres til det halve ved samtidig behandling. Omvendt sænkes plasmakoncentrationen (induktion af enzymet) ved behandling med fx carbamazepin eller phenobarbital, og samtidig behandling kræver derfor højere doser af lamotrigin.
Farmakokinetiske interaktioner udnyttes af og til farmakoterapeutisk. Probenecid, der i dag primært anvendes til behandling af artritis urica, er i sin tid udviklet som en booster af penicilliner. Probenecid øger plasmakoncentrationen af penicilliner og cefa-losporiner ved at hæmme den tubulære udskillelse af disse lægemidler. Flere andre lægemidlers udskillelse kan også hæmmes, herunder naproxen og indometacin. Proteasehæmmeren ritonavir, der anvendes i HIV-behandlingen, har kun en ganske beskeden anti-retroviral virkning. Ritonavir finder dog alligevel anvendelse i rationel behandling af HIV, da det er en kraftig hæmmer af CYP3A4 og derfor kan hæmme andre anti-retrovirale lægemidlers metabolisme. Herved øges disse andre antiretrovirale lægemidlers biotilgængelighed.
Lægemidlers interaktioner med andre substanser
Warfarin har et bredt interaktionspotentiale, både farmakokinetisk og farmakodynamisk. Også ved ændringer i forbruget af føde-varer kan warfarin påvirkes. Fx kan vitamin-K-holdige føde- varer, som fx kål, påvirke INR. Dette kombineret med warfarins relativt snævre terapeutiske interval og farlige bivirkninger gør warfarinbehandling potentielt risikabel. Derfor indstilles warfarin-behandling løbende efter måling af INR, og herved kan man kontrollere forskellige interaktioners effekt og regulere dosis af warfarin.
Tobak har primært farmakodynamisk interaktionspotentiale via virkningen på det parasympatiske nervesystem. Dog inducerer tobak også CYP1A2, der blandt andet er ansvarlig for metaboliseringen af flere antipsykotika. Opmærksomhed på bivirkninger af disse er derfor tilrådelig, når psykiatriske patienter i behandling med fx clozapin eller olanzapin forsøger rygestop eller genoptager rygning. Da denne interaktion er relateret til skadelige kulbrinter, er der ikke samme interaktion for nicotinsubstitutionspræparater.
Alkohol omsættes via enzymet alkoholdehydrogenase i leveren. Alkohol har kun ringe indvirkning på CYP-systemet. Medicin og alkohol har derfor meget lidt farmakokinetisk interaktionspotentiale, hvorimod de farmakodynamiske interaktioner er righoldige − fx med lægemidler med sedativ effekt. Dog inducerer alkohol CYP2E1, hvilket kan accelerere paracetamols omdannelse til en toksisk metabolit, hvilket kan have betydning i forbindelse ved samtidig alkohol- og paracetamolforgiftning.
Naturlægemidlers skæbne i organismen er generelt noget dårligere beskrevet end godkendte lægemidlers. Derfor er interaktionspotentialer også væsentligt dårligere belyst. Her skal blot nævnes nogle få. Perikon, der tages mod nedtrykthed og evt. depression, inducerer flere forskellige CYP-enzymer og kan således føre til behandlingssvigt af patientens øvrige medicin − fx amitriptylin. Ginko Biloba, der tages mod træthed, hukommelsesbesvær og perifere perfusionsproblemer, hæmmer CYP3A4 og kan føre til øgede plasmakoncentrationer af simvastain. Fiskeolie, der tages mod blodpropper, har blodfortyndende effekt og kan således medføre øget blødningstendens ved farmakodynamisk interaktion med trombocythæmmere, warfarin, NSAID mm.
Generelt har kosten ikke den store indflydelse på vores CYP-system. Dog kan mørkegrønne grønsager, som fx broccoli og kål, inducere CYP1A2, hvilket, som tidligere omtalt, kan have klinisk relevans i forbindelse med behandling med visse antipsykotika. Grapefrugtjuice er en relativt potent hæmmer af CYP3A4/5 selv ved moderat indtagelse, fx er 200 ml dagligt hyppigt anvendt i interaktionsstudier.
Interaktionsdatabasen
Interaktionsdatabasen (IDB) beskriver ca. 3.000 interaktioner mellem forskellige lægemidler samt naturlægemidler og vitamin- og mineralpræparater mm. Der kan enten søges på præparatets navn eller indholdsstof. Det vil dog altid være indholdsstofferne, der ses, uanset om der er søgt på det ene eller det andet. Der kan desuden vælges mellem en enkelt søgning, hvor man får alle kombinationer med ét præparat, eller en udvidet søgning, hvis man vil tjekke, hvordan to eller flere indholdsstoffer påvirker hinanden. Databasen indeholder en kort beskrivelse af alle interaktioner og en anbefaling til, hvordan lægen kan håndtere interaktionen. Det kan fx være at justere dosis. På basis af interaktionens potentielle sværhedsgrad, farvekodes denne som vist i figuren.
I databasen oplyses på basis af evt. beskrevne fund (objektive eller laboratorieværdier), hvorvidt interaktionen vurderes at have klinisk betydning, og dokumentationsgraden vægtes. Desuden er der mulighed for at se mere detaljerede oplysninger for hver interaktion, blandt andet i form af en kort gennemgang af den relevante litteratur med tilhørende referenceliste.
Andre opslagsværker
Stockley’s Drug Interactions er »biblen« inden for interaktionsrådgivning. Som i Interaktionsdatabasen gives råd og vejledning. Stockely’s udgives af Pharmaceutical Press, under The Royal Pharmaceutical Society. Der kan være diskrepans mellem Interakti-onsdatabasen og Stockley’s, da evidensen kan tolkes forskelligt.
Afdelingen for Klinisk Farmakologi på Indiana University udgiver og opdaterer deres P450 Drug Interactions Table. Her kan ses tabeller og evidens for lægemidlers affektion af forskellige CYP-enzymer.
Interaktionsdatabasen nu og i fremtiden
IDB blev oprindeligt etableret i perioden 2001-2003 i et samarbejde mellem Danmarks Apotekerforening, Den Almindelige Danske Lægeforening, Dansk Lægemiddelinformation A/S og Institut for Rationel Farmakoterapi. Siden 2004 har drift og vedligeholdelse af databasen været varetaget af Lægemiddelstyrelsen, nu Sundhedsstyrelsen, ved en arbejdsgruppe under Enhed for Læ-gemiddelovervågning og Medicinsk Udstyr. I 2009-2011 blev IDB kvalitetssikret med hjælp fra landets klinisk farmakologiske afdelinger.
Under ledelse af arbejdsgruppen opdateres IDB løbende med månedlig litteratursøgning efter henvendelser fra sundhedspersoner, myndigheder eller samarbejdspartnere samt ved opdaget diskrepans i forhold til andre opslagsværker − fx Stockleys Drug Interactions.
IDB’s primære evidensgrundlag er offentligt publicerede peer-reviewed original interaktionslitteratur (kliniske studier udført på mennesker og kasuistikker − ingen in vitro eller dyreforsøg) publiceret i PubMed og Embase. Databasen indeholder primært farmakokinetiske interaktioner, men medtager dog klinisk vigtige, ikke umiddelbart indlysende farmakodynamiske interaktioner.
Begrænsningen ved IDB er derfor, at teoretiske interaktioner og ikke-publicerede firmastudier ikke er medtaget. I 2014 ændredes IDB således, at nye lægemidler, for hvilke der ikke foreligger publicerede interaktionsstudier, men hvor lægemidlernes produktresuméer indeholder data herom, kom med i IDB med reference til disse. Heller ikke interaktioner med fødevarer (fraset nogle ganske få − grapefrugt og tranebærjuice), alkohol og tobak er medtaget. Der kan derfor være diskrepansoplysninger om interaktioner i produktresumeer, Pro.medicin.dk og IDB.
Der arbejdes pt. på integration af IDB med det fælles medicinkort (FMK) i forbindelse med lægemiddelordination. For nuværende er der to forskellige web-indgange for hhv. professionelle (www.interaktionsdatabasen.dk) og borgere (www.medicinkombination.dk). Sygehuse, apoteker og lægepraksis har mulighed for at integrere IDB i egne systemer ved at downloade den som XML-fil fra www.sundhedsstyrelsen.dk. Siden 2005 har IDB også været en integreret del af Medicinprofilen, således at Medicinprofilen automatisk tjekker for interaktioner mellem medicin, der er registreret i en medicinbrugers profil. Via Medicinprofilen udbydes data fra IDB også via en webservice. Denne anvendes af såvel Region Hovedstaden og Region Sjælland som lægepraksissystemet WinPLC.
Korrespondance
Kenneth Skov, kesk@dkma.dk.
Litteraturreferencer
Brøsen et al: Basal og Klinisk Farmakologi, 5. udgave, 2014.
Anglin R, Yuan Y, Moayyedi P, Tse F, Armstrong D, Leontiadis GI. Risk of upper gastrointestinal bleeding with selective serotonin reuptake inhibitors with or without concurrent nonsteroidal anti-inflammatory use: a systematic review and meta-analysis. Am J Gastroenterol. 2014 Jun;109(6):811-9.
Robbins N, Koch SE, Tranter M, Rubinstein J. The history and future of probenecid. Cardiovasc Toxicol. 2012 Mar;12(1):1-9.
Yamamoto Y, Takahashi Y, Imai K, Ikeda H, Takahashi M, Nakai M, Inoue Y, Kagawa Y. Influence of uridine diphosphate glucuronosyltransferase inducers and inhibitors on the plasma lamotrigine concentration in pediatric patients with refractory epilepsy. Drug Metab Pharmacokinet. 2015 Jan 23.
Hull MW, Montaner JS. Ritonavir-boosted protease inhibitors in HIV therapy. Ann Med. 2011 Aug;43(5):375-88.
Izzo AA. Drug interactions with St. John's Wort (Hypericum perforatum): a review of the clinical evidence. Int J Clin Pharmacol Ther. 2004 Mar;42(3):139-48.
Haen E. Drug-drug interactions: interactions between xenobiotics. Nervenarzt. 2014 Apr;85(4):417-26.
http://www.ema.europa.eu/ema/index.jsp?curl=pages/medicines/landing/epar_search.jsp&mid=WC0b01ac058001d124
http://produktresume.dk
www.pro.medicin.dk
www.interaktionsdatabasen.dk (www.sundhedsstyrelsen.dk)
Stockleys Drug Interactions, 10th ed. (bog)
Micromedex: http://www.micromedexsolutions.com/micromedex2/librarian/
CYP tabeller fra Indiana University: http://medicine.iupui.edu/clinpharm/DDIs/ClinicalTable.aspx