Behandling med protonpumpehæmmere - forbrugsmønstre, indikationer og behandlingsvarighed
Rationel farmakoterapi nr. 11, 2015
Månedsbladet opdateres ikke efter udgivelsen. Indholdet afspejler den aktuelle evidens på udgivelsestidspunktet.
Af Peter Fentz Haastrup og Dorte Ejg Jarbøl
Forskningsenheden for Almen Praksis, Institut for Sundhedstjenesteforskning, Syddansk Universitet
Protonpumpehæmmere (PPI) er den mest effektive type syrehæmmende medicin på markedet i Danmark. Der findes forskellige typer PPI, der alle virker på samme måde ved at hæmme det enzym i ventriklen, der producerer mavesyre.
Brug af PPI er udbredt, og på trods af, at PPI gennem årene er blevet markant billigere, og næsten al PPI-forbruget udgøres af generiske lægemidler, omsatte man i 2013 i primærsektoren PPI for 117 mio. kr. (heraf blev der udbetalt 45 mio. kr. i regionalt tilskud). I alt indløser over en halv million danskere en recept på PPI på bare et år. Kun 3 % af det samlede forbrug købes i håndkøb, og 94 % af forbruget stammer fra primærsektoren (1).
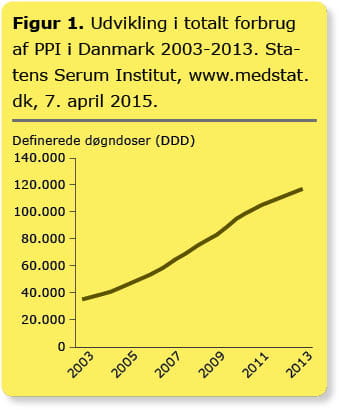
Lige siden omeprazol som den første PPI blev introduceret på markedet sidst i 1980’erne, er salget steget støt hvert år. Det totale salg af PPI i primærsektoren i Danmark er på ti år steget med 213 % (Figur 1). Samtidig er den gennemsnitlige individuelle mængde indløst PPI steget med 52 %, så hver medicinbruger i gennemsnit køber 224 døgndoser PPI på et år. Det tyder på, at antallet af langtidsbrugere (ofte defineret som patienter, der tager PPI i mere end to ud af seks måneder) er stigende (2).
Hvornår er langtidsbehandling indiceret?
Der er primært to grupper af patienter, hvor der er god evidens for langtidsbehandling (Tabel 1).
Den første gruppe er patienter med svær erosiv reflukssygdom (refluks-oeso-phagitis). Omkring 80 % af disse patienter vil opleve symptomrecidiv indenfor et år, hvis ikke de sættes i fast vedligeholdelsesbehandling med syrehæmmende medicin, ligesom der er risiko for udvikling af komplikationer, bl.a. i form af strikturer og dysplasi. Patienter med lette grader af erosioner (Los Angeles grad A-B) kan behandles med laveste dosis PPI, der giver sym-ptomkontrol, eller overgå til symptomstyret behandling (p.n.-behandling). Patienter med sværere grader af erosioner (Los Angeles grad C-D) bør behandles kontinuerligt med PPI i en dosis, der sikrer symptomkontrol (3).
Den anden gruppe, hvor langtidsbehandling med PPI er indiceret, er patienter med behov for forebyggelse af ulcus/ulcuskomplikationer forårsaget af behandling med ulcerogen medicin som f.eks. acetylsalicylsyre (ASA)/NSAID, og hvor seponering eller skift til anden behandling ikke er mulig. Samtidig behandling med PPI kan halvere risikoen for udvikling af ulcus i relation til ASA/NSAID-behandling (4).
Der findes flere risikofaktorer for udvikling af ulcuskomplikation hos patienter i ASA/NSAID-behandling (Tabel 2) (6), og risikoen for ulcus stiger med antallet af risikofaktorer. Risikoprofil og vurdering af behov for ulcusprofylakse må altid foretages individuelt for hver enkelt patient. Det er vigtigt forud for ordination af ASA/NSAID at identificere risikofaktorer og at gen-overveje indikationen hos risikopatienter. Hos risikopatienter, hvor ASA/NSAID-behandling er velindiceret, påbegyndes samtidig profylaktisk behandling med PPI, da en væsentlig del af ulcustilfældene ses hos patienter, der netop er påbegyndt ulcerogen medicin. Kortvarig behandling med NSAID giver ikke garanti for at undgå at inducere ulcus hos risikopatienter, ligesom ulcusprofylaktisk behandling med PPI kan reducere, men ikke fjerne risikoen for ulcuskomplikation (5).
Hvornår er langtidsbehandling ikke indiceret?
Den hyppigste årsag til dyspepsi i form af smerter eller ubehag i den øvre del af maven er funktionel dyspepsi, dvs. symptomer uden organisk forklaring (7). Her kan beroligelse og grundig information om tilstandens godartede natur være den bedste behandling, og farmakologisk behandling er ofte kun marginalt bedre end placebo (8).
Den næsthyppigste årsag til dyspepsi er reflukssygdom. Patienter med milde eller sporadiske symptomer kan behandles med syreneutraliserende antacida eller skumdannende alginater, der hindrer tilbageløb af mavesyre til spiserøret. Ved svære og hyppige reflukssymptomer behandles med PPI, hvor symptomstyret behandling anbefales (9, 10). Symptomstyret behandling er tidligere vist at kunne reducere PPI-forbruget til en tredjedel, uden det går ud over symptomkontrollen (11).
Patienter, der får konstateret ukompliceret ulcus (dvs. ulcus uden blødning, perforation eller penetration), tilbydes PPI som led i behandlingen i op til fire uger (6, 12). Herefter ophører behandlingen, medmindre såret ikke er helet, eller patienten fortsat har symptomer. Behandling af mavesår er således i langt de fleste tilfælde kortvarig, og kun ganske få patienter med mavesår har behov for langvarig behandling.
Er empirisk behandling med PPI problematisk?
Danske studier har vist, at hverken praktiserende læger eller gastroenterologer ud fra anamnese og objektiv undersøgelse er i stand til at forudsige, hvad gastroskopi vil vise hos en patient med dyspepsi (13). Alligevel anbefales det hverken i danske eller udenlandske guidelines at gastroskopere alle patienter med dyspepsi (6, 8). Vejledningerne fremhæver test for og behandling af infektion med mavesårsbakterien Helicobacter pylori som anbefalet udredningsstrategi frem for empirisk behandling med syrehæmmende medicin til patienter med dyspepsi uden faresignaler (6). På trods af dette bruges en kort behandling med PPI af og til som et diagnostisk redskab, forstået på den måde, at hvis patienten oplever effekt af behandlingen, vil det støtte ideen om, at patientens symptomer er syrerelaterede. Sådan en »PPI-test« er dog ikke i stand til hverken at diagnosticere eller udelukke årsager til symptomer fra øvre mavetarmkanal. Et positivt respons på behandlingsforsøget er ikke ensbetydende med, at symptomerne skyldes en syrerelateret lidelse, men kan være et udtryk for placeboeffekt eller for anden underliggende årsag til symptomerne.
Anbefalingen i dag er derfor, at patienter med faresignaler henvises til gastroskopi eller speciallæge (tabel 3) (8). Til udredning af voksne patienter med dyspepsi uden faresignaler er en Helicobacter pylori-test-and-eradicate-strategi sikker og omkostningseffektiv (8).
Ved at benytte en prøvebehandling med PPI til patienter med dyspepsi er der risiko for, at patienter fastholdes i et behov for vedvarende PPI-behandling, selvom der måske egentlig ikke er behov for syrehæmning.
Er PPI som langtidsbehandling problematisk?
PPI er generelt veltolererede lægemidler med få bivirkninger, men særligt ved langtidsbehandling kan der være risici. Epidemiologiske studier har bl.a. påvist en øget risiko for enteriske infektioner (14) og pneumoni (15). Ydermere er der fundet associationer mellem langtidsbrug af PPI og øget risiko for frakturer og hypomagnesiæmi (16), ligesom langtidsbrug indebærer risiko for polyfarmaci og mulige lægemiddelinteraktioner (17).
Vi ved endnu ikke nok om, hvad der ligger bag den kraftige stigning i PPI-forbruget, men fra flere steder peges der på et muligt overforbrug. Forekomsten af mavesår er stagnerende, og det samme gælder for behandling med ulcerogene lægemidler til ældre. En mulig forklaring på stigningen kan være en øget opmærksomhed på at identificere risikopatienter og ordinere PPI som ulcusprofylakse.
Rebound-fænomen
Nyere dansk forskning viser, at behandling med PPI i otte uger eller mere kan inducere et rebound-fænomen af ventriklens syreproduktion, som i sig selv kan give syrerelaterede symptomer efter ophør med medicinen (18). Disse symptomer kan fortsætte i mindst fire uger efter seponering af PPI. Årsagen til rebound-fænomenet skal findes i den hormonelle styring af ventriklens syreproduktion. Under normale omstændigheder styres parietalcellernes syreproduktion af hormonet gastrin, der indgår i en feedback-mekanisme med pH-værdien i mavesækken. Når man gennem længere tid har taget PPI og dermed bremset mavesyreproduktionen, ophobes gastrin i blodet. Når hæmningen af syrepumpen forsvinder, fremkaldes en meget kraftig syreproduktion, der kan forårsage syrerelaterede symptomer. Hvis man ikke er opmærksom på dette fænomen, kan både patient og behandler tænke, at symptomer opstået ved seponering af medicinen må betyde et fortsat behov for syre-hæmning. Dette rebound-fænomen kan altså være en medvirkende årsag til, at patienten bliver »afhængig« og fastholdes i et behov for vedvarende PPI-behandling, selvom der måske slet ikke er noget reelt behov.
Kan patienter i langtidsbehandling stoppe igen?
En nylig gennemgang af litteraturen på området (inklusive to danske studier) viser, at det er muligt at identificere et betydeligt antal patienter, der bliver behandlet med PPI uden oplagt årsag. Efter forskellige tiltag (f.eks. information og vejledning i aftrapning) er mellem 14 og 64 % af disse patienter i stand til at ophøre med medicinen uden forværring i symptomer. Dertil kommer, at mellem 30 og 50 % kan nedsætte dosis af behandlingen. Langsom aftrapning af medicinen ser ud til at være mere effektivt end brat ophør, hvilket kan afspejle den kliniske relevans af hypergastrinæmi og rebound-hypersekretion (19). Dette støttes yderligere af, at serum-gastrin-niveau findes som en uafhængig prædiktor, for at seponeringsforsøg mislykkes (20). Ved forsøg på seponering/dosisreduktion er det derfor relevant at gøre patienten opmærksom på risikoen for syrerelaterede symptomer i mindst fire uger efter ophør, hvilket ikke nødvendigvis er udtryk for behov for at genoptage behandlingen. Ofte kan det være relevant med antacidum/alginat til at kupere syresymptomerne. Ved behov for genoptagelse af PPI-behandling kan symptomstyret behandling ofte være tilstrækkeligt.
Korrespondance
Dorte Ejg Jarbøl, djarbol@health.sdu.dk.
Litteraturreferencer
1. http://medstat.dk/. Statens Serum Institut; [cited 2015 August 12].
2. Haastrup P, Paulsen MS, Zwisler JE, Begtrup LM, Hansen JM, Rasmussen S, et al. Rapidly increasing prescribing of proton pump inhibitors in primary care despite interventions: a nationwide observational study. The European journal of general practice. 2014;20(4):290-3.
3. Tytgat GN. Review article: management of mild and severe gastro-oesophageal reflux disease. Alimentary pharmacology & therapeutics. 2003;17 Suppl 2:52-6.
4. Targownik LE, Metge CJ, Leung S, Chateau DG. The relative efficacies of gastroprotective strategies in chronic users of nonsteroidal anti-inflammatory drugs. Gastroenterology. 2008;134(4):937-44.
5. Lanza FL, Chan FK, Quigley EM. Guidelines for prevention of NSAID-related ulcer complications. The American journal of gastroenterology. 2009;104(3):728-38.
6. Dyspepsi - udredning og behandling af voksne med symptomer fra øvre mave-tarm-kanal. København: Dansk Selskab for Almen Medicin 2009.
7. Hansen JM, Bytzer P, Schaffalitzky de Muckadell OB. Placebo-controlled trial of cisapride and nizatidine in unselected patients with functional dyspepsia. The American journal of gastroenterology. 1998;93(3):368-74.
8. Talley NJ, Vakil N. Guidelines for the management of dyspepsia. The American journal of gastroenterology. 2005;100(10):2324-37.
9. Pace F, Porro GB. On-demand PPI therapy in GERD. Current treatment options in gastroenterology. 2008;11(1):35-42.
10. Pace F, Tonini M, Pallotta S, Molteni P, Porro GB. Systematic review: maintenance treatment of gastro-oesophageal reflux disease with proton pump inhibitors taken 'on-demand'. Alimentary pharmacology & therapeutics. 2007;26(2):195-204.
11. Tsai HH, Chapman R, Shepherd A, McKeith D, Anderson M, Vearer D, et al. Esomeprazole 20 mg on-demand is more acceptable to patients than continuous lansoprazole 15 mg in the long-term maintenance of endoscopy-negative gastro-oesophageal reflux patients: the COMMAND Study. Alimentary pharmacology & therapeutics. 2004;20(6):657-65.
12. pro.medicin.dk. Ulcussygdom 2014 [updated 29.12.2014; cited 2015 October 12]. Available from: http://pro.medicin.dk/Sygdomme/Sygdom/318223
13. Hansen JM, Bytzer P, Schaffalitzky De Muckadell OB. Management of dyspeptic patients in primary care. Value of the unaided clinical diagnosis and of dyspepsia subgrouping. Scandinavian journal of gastroenterology. 1998;33(8):799-805.
14. McDonald EG, Milligan J, Frenette C, Lee TC. Continuous Proton Pump Inhibitor Therapy and the Associated Risk of Recurrent Clostridium difficile Infection. JAMA internal medicine. 2015;175(5):784-91.
15. Sarkar M, Hennessy S, Yang YX. Proton-pump inhibitor use and the risk for community-acquired pneumonia. Annals of internal medicine. 2008;149(6):391-8.
16. Hess MW, Hoenderop JG, Bindels RJ, Drenth JP. Systematic review: hypomagnesaemia induced by proton pump inhibition. Alimentary pharmacology & therapeutics. 2012;36(5):405-13.
17. Moayyedi P, Leontiadis GI. The risks of PPI therapy. Nature reviews Gastroenterology & hepatology. 2012;9(3):132-9.
18. Reimer C, Sondergaard B, Hilsted L, Bytzer P. Proton-pump inhibitor therapy induces acid-related symptoms in healthy volunteers after withdrawal of therapy. Gastroenterology. 2009;137(1):80-7, 7 e1.
19. Haastrup P, Paulsen MS, Begtrup LM, Hansen JM, Jarbol DE. Strategies for discontinuation of proton pump inhibitors: a systematic review. Family practice. 2014;31(6):625-30.
20. Bjornsson E, Abrahamsson H, Simren M, Mattsson N, Jensen C, Agerforz P, et al. Discontinuation of proton pump inhibitors in patients on long-term therapy: a double-blind, placebo-controlled trial. Alimentary pharmacology & therapeutics. 2006;24(6):945-54.