Farmakologisk behandling af akutte smertetilstande i bevægeapparatet
Artikel fra Rationel Farmakoterapi 8, 2020
Månedsbladet opdateres ikke efter udgivelsen. Indholdet afspejler den aktuelle evidens på udgivelsestidspunktet.
Marie Lund1, Gitte Krogh Madsen2, Jens Gram-Hansen3 og Mogens Pfeiffer-Jensen4
1) Klinisk Farmakologisk Afdeling, Bispebjerg og Frederiksberg Hospital, og Center for Evidens, Uddannelse og Beredskab, Sundhedsstyrelsen
2) Roskilde Lægehus
3) Praksisvikar og Praksiskonsulent, Silkeborg
4) Videncenter for Reumatologi og Rygsygdomme, Rigshospitalet – Glostrup
Denne artikel giver et overblik over farmakologisk smertebehandling af akutte muskuloskeletale smertetilstande i almen praksis med fokus på nyeste viden om effekt og bivirkninger.
Afgrænsning
Akutte muskuloskeletale smertetilstande dækker over smerter, som udgår fra bevægeapparatet. Det er hyppigt præsenterede symptomer i almen praksis. Her fokuseres på patienter med nociceptive smerter på grund af overbelastninger, traumer, degenerationer, inflammationer (bursitter, tendinoser/tendinitter, artritter) og infektioner. Smerter med baggrund i nervepåvirkning (neurogene/neuropatiske smerter) samt postoperative smerter er ikke medtaget i denne gennemgang.
Anbefalingerne i denne artikel bygger blandt andet på viden fra en række nylige udgivelser, herunder evidensgennemgangen fra Den Nationale Rekommandationsliste vedr. farmakologisk behandling af akutte muskuloskeletale smerter [1] og Smerteguiden [2]. Vi fokuserer på farmakologisk behandling af smertetilstande af maksimalt 14 dages varighed i denne artikel. Det bemærkes, at der i Den Nationale Rekommandationsliste [1] og i Smerteguiden [2] er anvendt en væsentligt længere tidsramme. Denne artikel beskæftiger sig ikke med farma-kologisk smertebehandling under graviditet og amning; her henvises til tidligere artikler i Månedsbladet om emnerne [3-5]. Se Faktaboks for opsummering af initial udredning, diagnostik og behandling.
Farmakologisk behandling af akutte muskuloskeletale smerter
Præcis diagnostik af årsagerne til den smerteudløsende vævsbeskadigelse/påvirkning skal afklares samtidigt med, at smertebehandlingen påbegyndes [1]. Hvis der findes kausal behandling, skal denne selvfølgelig primært iværksættes. Farmakologisk smertebehandling skal betragtes som symptomatisk behandling og bør altid været suppleret af information og non-farmakologisk behandling.
Generelt er effekten af analgetika ved akutte muskuloskeletale smerter relativt sparsom og/eller begrænset af bivirkninger. Generelt bør smertestillende behandling primært bestå af paracetamol, men ved flere inflammatoriske tilstande er non-selektive NSAID fortsat en vigtig symptomlindrende behandlingsmulighed. Opioider vil sjældent være indiceret til akutte muskuloskeletale smertetilstande.
Evidens for virkning
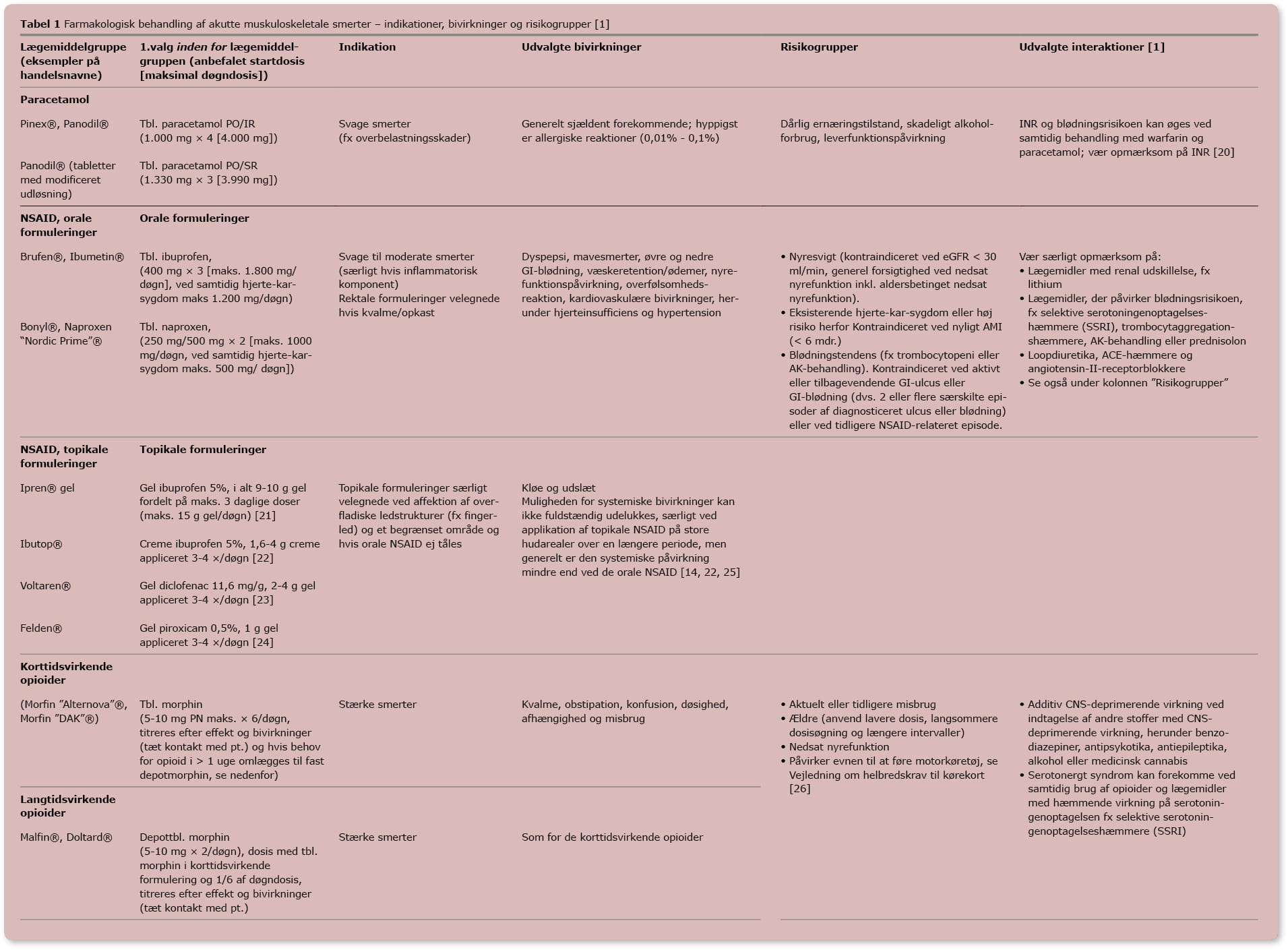
Overordnet gælder, at der findes få randomiserede studier af høj videnskabelig kvalitet, som undersøger effekten af farmakologisk behandling af akutte muskuloskeletale smertetilstande. Mange analgetika er til gengæld velundersøgte ved forskellige akutte postoperative smertetilstande. Varigheden af disse studier er dog oftest forholdsvis kort, og langt størsteparten af studierne er enkeltdosisstudier [1]. I mangel af bedre kan førnævnte studier dog bruges til at give et fingerpeg om forventet effekt blandt patienter med akutte muskuloskeletale smerter, idet postoperative smertetilstande også er af nociceptiv karakter. Tabel 1 indeholder en generel oversigt over lægemidler inden for de forskellige lægemiddelgrupper inkl. dosering, indikationer, hyppigste bivirk-ninger og udvalgte risikogrupper.
Paracetamol
Paracetamol er undersøgt i et randomiseret, kontrolleret klinisk studie af Williams et al [6] til patienter med nyopståede akutte lænde-ryg-smerter af mindst moderat karakter. Sammenlignet med placebo viste studiet ingen yderligere effekt af paracetamol på hverken smerteintensitet eller funktionsevne, men heller ikke øget -forekomst af alvorlige bivirkninger. Hvis der ekstrapoleres fra enkeltdosisstudier, tyder studier af patienter med akutte postoperative smerter dog samlet set på en acceptabel effekt af paracetamol til patienter med disse smertetilstande: number needed to treat (NNT) på 4-6. Samtidig har paracetamol hos ikke-risikopatienter en acceptabel bivirkningsprofil (for risikopatienter: se Tabel 1). Derfor er paracetamol i vores optik fortsat et udmærket førstevalg ved svage akutte muskuloskeletale smertetilstande, hvis man følger op på effekt og bivirkninger og seponerer ved manglende effekt efter 2-4 dages behandling [1].
NSAID
Der er ikke dokumenteret klinisk betydende forskelle i effekten mellem de mange forskellige NSAID til akutte muskuloskeletale smertetilstande, men der er forskelle i stoffernes bivirkningsprofiler, fx mht. gastrointestinale (GI) og kardiovaskulære (CV) bivirkninger [1]. Det er, som altid, vigtigt at vurdere effekt og bivirkninger og tage stilling til evt. risikofaktorer. Generelt bør NSAID bruges i lavest mulig dosis og i kortest mulig tid [1, 7]. Alle NSAID virker ved at hæmme enzymet cyclooxygenase (COX) og dermed syntesen af prostaglandiner, prostacykliner og tromboxaner [8]. Der er beskrevet hæmning af mindst to isoenzymer, COX1 og COX2. Effekten af NSAID er analgetisk, antipyretisk og antiinflammatorisk [1, 7].
Orale NSAID
Et stort Cochrane-review om akutte lænde-ryg-smerter finder overordnet sparsom evidens for klinisk relevant effekt: Ved behandling med et NSAID ≤ 2 uger var forskellen sammenlignet med placebo –6,4 (–10,2 til –2,5) på en visuel analog skala (VAS) fra 0 til 100 [1].
Et systematisk review og metaanalyse undersøger effekten af NSAID til behandling af ankelforstuvninger og finder overordnet sparsom evidens for klinisk relevant effekt; når patienterne blev behandlet med et oralt administreret NSAID inden for 72 timer efter skadens opståen, sås sammenlignet med placebo en reduktion i smerteintensitet på –9,0 (–10,8 til –7,2) på en VAS fra 0 til 100 [9].
Generelt er evidensen om forekomsten af alvorlige GI-bivirkninger ved korttidsbehandling med NSAID af sparsom kvalitet. Et ældre studie [10] rapporterer, at begyndende GI-erosioner kan ses efter 2 uger, og at der går 1-3 måneder, før der ses manifest ulcus. Baseret på klinisk erfaring optræder de velkendte bivirkninger i form af dyspepsi og mavesmerter ofte allerede efter få dages behandling, men synes ikke at have prædiktiv værdi for senere udvikling af ulcus [11]. Generelt stiger risikoen for bivirkninger ved NSAID med behandlingsvarighed og -dosis. Ved risikofaktorer for ulcuskomplikation er det god klinisk praksis at supplere med syrepumpehæmmere, hvis NSAID-behandling er påkrævet [1, 7]. For risikofaktorer for ulcuskomplikation ved NSAID-behandling se Tabel 2, og for kontraindikationer i relation til tidligere ulcus se Tabel 1.
Data om CV-bivirkninger i relation til NSAID er ligeledes sparsomme, men observationelle studier tyder på, at selv kortvarig behandling med NSAID (i nogle studier under en uge) er associeret til øget risiko for død og genindlæggelse efter myo-kardieinfarkt [12]. Se Tabel 2 for opsummering af præparatvalg for de orale formuleringer af NSAID og risikofaktorer for GI-blødning og hjerte--kar-sygdom.
NSAID påvirker den renale blodgennemstrømning gennem kontraktion af den afferente arteriole i glomerulus. Dvs. man skal særligt være opmærksom hos patienter med kronisk nedsat nyrefunktion (se Tabel 2), men også ved samtidig behandling med andre lægemidler, der påvirker den renale blodgennemstrømning (fx ACE-hæmmere, angiotensin-II-receptorblokkere og loopdiuretika) [13]. NSAID hæmmer trombocytterne, dvs. der er øget risiko for blødning ved samtidig brug af antikoagulantia eller trombocytaggregationshæmmere [1].
Topikale NSAID
Topikale/lokalt applicerede NSAID bruges til et bredt spektrum af smerte-tilstande som fx forstrækninger og forstuvninger, tendinopatier eller lokale muskelsmerter.
Seneste Cochrane-review, der inkluder 260 studier med i alt omkring 30.700 patienter, anfører god evidens for effekt af forskellige topikale formuleringer af diclofenac på akutte smertetilstande som forstuvninger og forstrækninger, hvor der fandtes lav NNT mellem 2 og 5. Bivirkningsfrekvensen var lav (4,3%) og på niveau med frekvensen ved placebo [14].
Rektale NSAID
Der er ikke fundet evidens vedr. rektale formuleringer af NSAID som led i evidensgennemgangen for Den Nationale Rekommandationsliste vedr. farm-akologisk behandling af akutte muskuloskeletale smerter [1], men rektale formuleringer af NSAID kan være velegnede ved samtidig kvalme/opkast. Her kan man anvende supp. naproxen 500 mg per dag (maks. 1.000 mg/dag, ved samtidig hjerte-kar-sygdom maks. 500 mg per dag) [1]. Der gælder de samme forholdsregler mht. GI-bivirkninger for rektal som for oral administration [15].
Opioider
Generelt vil det være et fåtal af akutte muskuloskeletale smertetilstande, hvor der i almen praksis er indikation for behandling med et opioid. Hvis der findes indikation herfor (fx svære smertetilstande i forbindelse med knoglebrud, der ikke har krævet operation, svære distorsioner/kontusioner såsom fx contusio thoracis, osteoporo-tiske sammenfald, hvor behovet for smertebehandling typisk strækker sig ud over de 14 dage, eller ved akutte lændesmerter med eller uden nerve-påvirkning), er morphin førstevalg [2]. Alle opioider har potentiale for afhængighed, og patienter i behandling med opioider bør følges tæt og systematisk. For yderligere information henvises til Sundhedsstyrelsens Vejledning om ordination af afhængighedsskabende lægemidler [16] og til den nationale kliniske retningslinje om systematisk opfølgning af patienter i behandling med opioider for non-maligne smerter [17]. Behandling med opioider bør suppleres med laksantia for at modvirke obstipation. Dette er fx forebyggende behandling med osmotisk virkende laksantia, evt. suppleret med peristaltikfremmende laksantia [18]. Ved forventet behandlingsvarighed < 1 uge startes med korttidsvirkende opioider. Ved forventet behandlingsvarighed ≥ 1 uge startes med langtidsvirkende opioider [1, 2].
Nedsat nyrefunktion
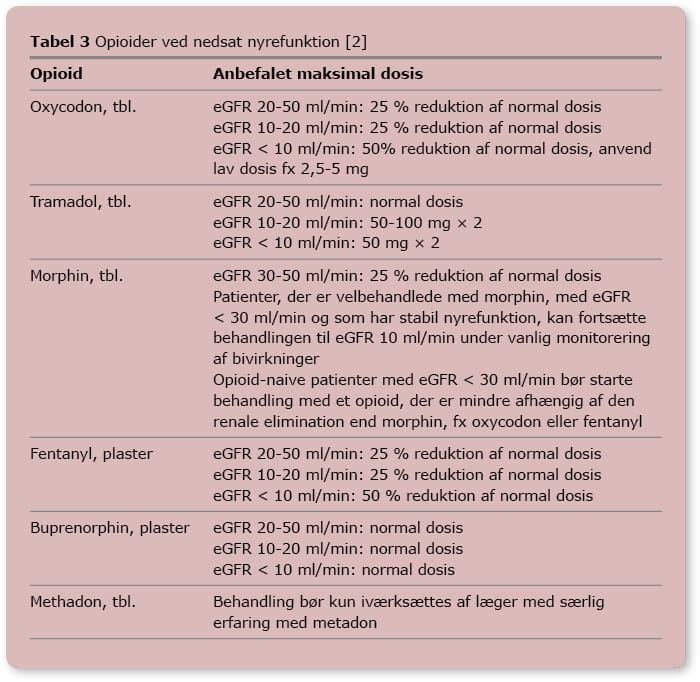
Ved nedsat nyrefunktion bør man generelt være forsigtig ved brug af opioider og huske på, at der er brug for dosisjustering ved progredierende nyreinsufficiens. For anbefalinger om valg af opioid og dosering ved nedsat nyrefunktion, se Tabel 3 (Tabel 3 er kun elektronisk tilgængelig).
Kombinationspræparater
Der er yderst sparsom evidens for brug af kombinationspræparater til akutte muskuloskeletale smerte-tilstande [1]. Her tænkes specifikt på Ketogan (ketobemidon og dimethylaminodiphenylbuten), Kodipar (codein og paracetamol), Treo (acetylsalicylsyre og caffein), Panodil Extra (paracetamol og caffein), Kodamid (codein, caffein, magnesium, propyphenazon og salicylamid) og Kodimagnyl (acetylsalicylsyre, codein og magnesiumoxid). Generelt gælder, at de kombinationspræparater, der indeholder codein eller acetylsalicylsyre, ikke anbefales: 1) codein, fordi der er sparsom dokumentation for effekt blandt patienter med akutte muskuloskeletale smerter, og fordi 10% af befolkningen ikke kan omsætte codein til den aktive metabolit, og 2) acetylsalisylsyre, fordi det generelt ikke længere anses for at have en plads i behandlingen af akutte muskuloskeletale smerter. Endvidere gælder, at der generelt er sparsom evidens for at tillægge caffein som analgetisk adjuvans i behandlingen af akutte muskuloskeletale smerter.
Tabel 1
| Lægemiddel-gruppe (eksempler på handelsnavne) |
1. valginden forlægemiddel-gruppen (anbefalet startdosis [maksimal døgndosis]) |
Indikation | Udvalgte bivirkninger | Risiko-grupper | Udvalgte interaktioner [1] |
| Paracetamol |
|
Svage smerter (fx overbelastningsskader) | Generelt sjældent forekommende; hyppigst er allergiske reaktioner (0,01% - 0,1%) | Dårlig ernæringstilstand, skadeligt alkoholforbrug, leverfunktionspåvirkning |
INR og blødningsrisikoen kan øges ved samtidig behandling med warfarin og paracetamol; vær opmærksom på INR [20] |
| Pinex® | Tbl. paracetamol PO/IR (1.000 mg × 4 [4.000 mg]) | ||||
| Panodil® (tabletter med modificeret udløsning | Tbl. paracetamol PO/SR (1.330 mg × 3 [3.990 mg]) |
|
Lægemiddel-gruppe (eksempler på handelsnavne) |
1. valg inden for lægemiddel-gruppen (anbefalet startdosis [maksimal døgndosis]) |
Indikation | Udvalgte bivirkninger | Risiko-grupper | Udvalgte interaktioner [1] |
| NSAID, orale formuleringer | Orale formuleringer | Svage til moderate smerter (særligt hvis inflammatorisk komponent) Rektale formuleringer velegnede hvis kvalme/opkast |
Dyspepsi, mavesmerter, øvre og nedre GI-blødning, væskeretention/ødemer, nyrefunktionspåvirkning, overfølsomhedsreaktion, kardiovaskulære bivirkninger, herunder hjerteinsufficiens og hypertension |
|
Vær særligt opmærksom på:
|
| Brufen®, Ibumetin® | Tbl. ibuprofen, (400 mg × 3 [maks. 1.800 mg/ døgn], ved samtidig hjerte-kar-sygdom maks 1.200 mg/døgn) |
|
|||
| Bonyl®, Naproxen “Nordic Prime”® | Tbl. naproxen, (250 mg/500 mg × 2 [maks. 1000 mg/døgn, ved samtidig hjerte-karsygdom maks. 500 mg/ døgn]) |
|
|
| Lægemiddel-gruppe (eksempler på handelsnavne) | 1. valg inden for lægemiddel-gruppen (anbefalet startdosis [maksimal døgndosis]) |
Indikation | Udvalgte bivirkninger | Risiko-grupper | Udvalgte interaktioner [1] |
| NSAID, topikale formuleringer | Topikale formuleringer | Topikale formuleringer særligt velegnede ved affektion af overfladiske ledstrukturer (fx fingerled) og et begrænset område og hvis orale NSAID ej tåles |
Kløe og udslæt Muligheden for systemiske bivirkninger kan ikke fuldstændig udelukkes, særligt ved applikation af topikale NSAID på store hudarealer over en længere periode, men generelt er den systemiske påvirkning mindre end ved de orale NSAID [14, 22, 25] |
||
| Ipren® gel | Gel ibuprofen 5%, i alt 9-10 g gel fordelt på maks. 3 daglige doser (maks. 15 g gel/døgn) [21] | ||||
| Ibutop® | Creme ibuprofen 5%, 1,6-4 g creme appliceret 3-4 ×/døgn [22] | ||||
| Voltaren® | Gel diclofenac 11,6 mg/g, 2-4 g gel appliceret 3-4 ×/døgn [23] |
||||
| Felden® | Gel piroxicam 0,5%, 1 g gel appliceret 3-4 ×/døgn [24] |
|
Lægemiddel-gruppe (eksempler på handelsnavne) |
1. valg inden for lægemiddel-gruppen (anbefalet startdosis [maksimal døgndosis]) |
Indikation | Udvalgte bivirkninger | Risiko-grupper | Udvalgte interaktioner [1] |
| Korttidsvirkende opioider | Stærke smerter | Kvalme, obstipation, konfusion, døsighed, afhængighed og misbrug |
|
|
|
| (Morfin ”Alternova”®, Morfin ”DAK”®) | Tbl. morphin (5-10 mg PN maks. × 6/døgn, titreres efter effekt og bivirkninger (tæt kontakt med pt.) og hvis behov for opioid i > 1 uge omlægges til fast depotmorphin, se nedenfor) |
|
Lægemiddel-gruppe (eksempler på handelsnavne) |
1. valg inden for lægemiddel-gruppen (anbefalet startdosis [maksimal døgndosis]) |
Indikation | Udvalgte bivirkninger | Risiko-grupper | Udvalgte interaktioner [1] |
| Langtidsvirkende opioider | Stærke smerter | Kvalme, obstipation, konfusion, døsighed, afhængighed og misbrug |
|
|
|
| Malfin®, Doltard® |
Depottbl. morphin (5-10 mg × 2/døgn), dosis med tbl. morphin i korttidsvirkende formulering og 1/6 af døgndosis, titreres efter effekt og bivirkninger (tæt kontakt med pt.) |
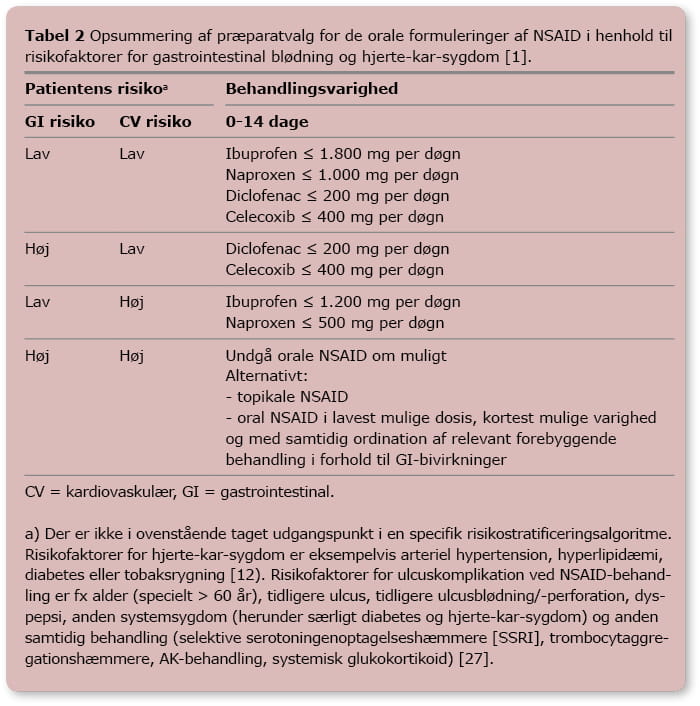
Tabel 2
Opsummering af præparatvalg for de orale formuleringer af NSAID i henhold til risikofaktorer for gastrointestinal blødning og hjerte-kar-sygdom [1].
| Patientens risikoa |
Behandlingsvarighed | |
| GI risiko | CV risiko | 0-14 dage |
| Lav | Lav | Ibuprofen ≤ 1.800 mg per døgn Naproxen ≤ 1.000 mg per døgn Diclofenac ≤ 200 mg per døgn Celecoxib ≤ 400 mg per døgn |
| Høj | Lav |
Diclofenac ≤ 200 mg per døgn Celecoxib ≤ 400 mg per døgn |
| Lav | Høj |
Ibuprofen ≤ 1.200 mg per døgn Naproxen ≤ 500 mg per døgn |
| Høj | Høj | Undgå orale NSAID om muligt Alternativt: - topikale NSAID - oral NSAID i lavest mulige dosis, kortest mulige varighed og med samtidig ordination af relevant forebyggende behandling i forhold til GI-bivirkninger |
CV = kardiovaskulær, GI = gastrointestinal.
a) Der er ikke i ovenstående taget udgangspunkt i en specifik risikostratificeringsalgoritme. Risikofaktorer for hjerte-kar-sygdom er eksempelvis arteriel hypertension, hyperlipidæmi, diabetes eller tobaksrygning [12). Risikofaktorer for ulcuskomplikation ved NSAID-behandling er fx alder (specielt > 60 år), tidligere ulcus, tidligere ulcusblødning/-perforation, dyspepsi, anden systemsygdom (herunder særligt diabetes og hjerte-kar-sygdom) og anden samtidig behandling (selektive serotoningenoptagelseshæmmere [SSRI], trombocytaggregationshæmmere, AK-behandling, systemisk glukokortikoid) [27].
Opsummering
- Farmakologisk smertebehandling er symptomatisk og bør altid være suppleret af
information og non-farmakologisk behandling. - Ved indikation for farmakologisk smertebehandling:
1. Valg: tbl. paracetamol, 1 g × 4 daglig, generelt ringe dokumentation for effekt,
men kan forsøges pga. få bivirkninger hos ikke-risikopatienter✱.
2. Valg: NSAID (fx topikal eller tbl. ibuprofen 400 mg × 3 daglig✱✱), velegnet særligt til de akutte smertetilstande med inflammatorisk komponent, brug lavest
mulige dosis i kortest mulige varighed pga. risiko for bivirkninger.
3. Ved utilstrækkelig effekt af paracetamol og/eller NSAID og stærke smerter kan
suppleres med et opioid (fx tbl. morphin), kræver tæt opfølgning og er forbeholdt en lille gruppe patienter.
✱ Med risikopatienter menes fx patienter med dårlig ernæringstilstand, skadeligt
alkoholforbrug og leverfunktionspåvirkning [1].
✱✱ Vurdering af gavnlige vs. skadelige virkninger for den enkelte patient (hjerte-karsygdom, tidligere ulcus og risikofaktorer for GI-blødning, nyrefunktion m.m.), evt.
suppleret med protonpumpehæmmer.
Tabel 3
Opioider ved nedsat nyrefunktion [2]
Opioid-naive patienter med eGFR < 30 ml/min bør starte behandling med et opioid, der er mindre afhængig af den renale elimination end morphin, fx oxycodon eller fentanyl| Opioid | Anbefalet maksimal dosis |
| Oxycodon, tbl. |
eGFR 20-50 ml/min: 25 % reduktion af normal dosis eGFR 10-20 ml/min: 25 % reduktion af normal dosis eGFR < 10 ml/min: 50% reduktion af normal dosis, anvend lav dosis fx 2,5-5 mg |
| Tramadol, tbl. |
eGFR 20-50 ml/min: normal dosis eGFR 10-20 ml/min: 50-100 mg × 2 eGFR < 10 ml/min: 50 mg × 2 |
| Morphin, tbl. |
eGFR 30-50 ml/min: 25 % reduktion af normal dosis Patienter, der er velbehandlede med morphin, med eGFR < 30 ml/min og som har stabil nyrefunktion, kan fortsætte behandlingen til eGFR 10 ml/min under vanlig monitorering af bivirkninger Opioid-naive patienter med eGFR < 30 ml/min bør starte behandling med et opioid, der er mindre afhængig af den renale elimination end morphin, fx oxycodon eller fentanyl |
| Fentanyl, plaster |
eGFR 20-50 ml/min: 25 % reduktion af normal dosis eGFR 10-20 ml/min: 25 % reduktion af normal dosis eGFR < 10 ml/min: 50 % reduktion af normal dosis |
| Buprenorphin, plaster |
eGFR 20-50 ml/min: normal dosis eGFR 10-20 ml/min: normal dosis eGFR < 10 ml/min: normal dosis |
| Methadon, tbl. |
Behandling bør kun iværksættes af læger med særlig erfaring med metadon |
Faktaboks
Initial udredning, diagnostik og behandling af akutte muskuloskeletale smerter i almen praksis
- Primære udredning: Anamnese inkl. smerteanalyse og objektiv undersøgelse.
- Behandlingsplan: Laves på baggrund af diagnose, prognose, komorbiditet, komplians, erhverv og dokumenterede behandlingsmodaliteter.
- Ofte er non-farmakologisk tilgang tilstrækkelig med fokus på information om diagnose, forventet forløb og råd om øvelser/træning.
- Den analgetiske behandling bør bygge på en smerteanalyse med stillingtagen til, om det drejer sig om nociceptive og/eller neuropatiske smerter.
- Der kan suppleres med analgetika [19], se afsnittet ”Farmakologisk behandling af akutte muskuloskeletale smerter”.
- Husk: Patienten bør være velinformeret om diagnose, sygdomsforløb, prognose og behandling, herunder forventet effekt og bivirkninger med henblik på, at der sættes et realistisk behandlingsmål.
- Behandlingen bør løbende monitoreres med vurdering af behandlingseffekt (fx VAS-score) og bivirkninger.
- Behandlingsmålet er smertelindring og om muligt at standse den farmakologiske behandling < 14 dage.
Referencer
- Sundhedsstyrelsen. Den Nationale Rekommandationsliste. Akutte muskuloskeletale smerter. 2020.
- Region Midtjylland, Region Hovedstaden, Region Nordjylland, Region Sjælland, Region Syddanmark. Indsatser for Rationel Farmakoterapi, Sundheds-styrelsen. Smerteguiden. 2019.
- Haastrup MB. Smertestillende medicin til gravide. Månedsbladet Rationel Farmakoterapi 2016;(5).
- Futtrup TB, Andersen JT. Hyppige farmakologiske problemstillinger i svangerskabet. Rationel Farmakoterapi 2019;(6).
- Andersen JT, Futtrup TB. Lægemidler og amning. Rationel Farmakoterapi 2018;(7).
- Williams CM, Maher CG, Latimer J et al. Efficacy of paracetamol for acute low-back pain: a double-blind, randomised controlled trial. Lancet 2014;384:1586-96.
- Indsatser for Rationel Farmakoterapi, Sundheds-styrelsen. Den Nationale Rekommandationsliste. Farmakologisk behandling af kroniske nociceptive smerter. 2018.
- Vane JR. Inhibition of prostaglandin synthesis as a mechanism of action for aspirin-like drugs. Nat New Biol 1971;231:232-5.
- van den Bekerom MPJ, Sjer A, Somford MP et al. Non-steroidal anti-inflammatory drugs (NSAIDs) for treating acute ankle sprains in adults: benefits outweigh adverse events. Knee Surg Sports Traumatol Arthrosc 2015;23:2390-9.
- McCarthy DM. Nonsteroidal antiinflammatory drug-induced ulcers: management by traditional therapies. Gastroenterology 1989;96:662-74.
- Hollenz M, Stolte M, Leodolter A et al. NSAID-associated dyspepsia and ulcers: a prospective cohort study in primary care. Dig Dis 2006;24:189-94.
- Dansk Cardiologisk Selskab. DCS Holdningspapir: NSAID behandling hos patienter med hjertekarsygdom. Holdningspapir 2016;(1).
- Schougaard Christiansen ML, Gregersen T, Siersbæk M. Lægemiddelinteraktioner i almen praksis. Rationel Farmakoterapi 2020;(2).
- Derry S, Wiffen PJ, Kalso EA et al. Topical analgesics for acute and chronic pain in adults – an overview of Cochrane reviews. Cochrane Database Syst Rev 2017;5:CD008609.
- Lægemiddelstyrelsen. Produktresumé Bonyl, suppositorier (31. mar 2016).
- Sundhedsstyrelsen. Vejledning om ordination af afhængighedsskabende lægemidler (VEJ nr 9009 af 27/12/2013). 2013.
- Dansk Selskab for Anæstesiologi og Intensiv Medicin. Puljefinansieret NKR: Systematisk opfølgning af patienter i behandling med opioider for non-maligne smerter. 2019.
- Basislisten – lægemiddelanbefalinger i Region Sjælland – obstipation. www.sundhed.dk/sundhedsfaglig/information-til-praksis/sjaelland/almen-praksis/laegemidler/
basislisten-sjaelland/obstipation/ (9. mar 2020). - Reumatologi. 4. udg. FADL’s Forlag.
- Lægemiddelstyrelsen.
www.interaktionsdatabasen.dk. “paracetamol” og “warfarin” (30. maj 2020). - Lægemiddelstyrelsen. Produktresumé Ipren, gel 5% (17. mar 2015).
- Lægemiddelstyrelsen. Produktresumé Ibutop, creme 5% (1. jun 2016).
- Lægemiddelstyrelsen. Produktresumé Voltaren gel (15. okt 2013).
- Lægemiddelstyrelsen. Produktresumé Felden gel 0,5% (19. maj 2016).
- Derry S, Moore RA, Gaskell H et al. Topical NSAIDs for acute musculoskeletal pain in adults. Cochrane Database Syst Rev 2015;6:CD007402.
- Styrelsen for Patientsikkerhed. Vejledning om helbredskrav til kørekort (version 1.0).
- Haastrup PF, Jarbøl DE. Behandling med protonpumpehæmmere - forbrugsmønstre, indikationer og behandlings-varighed. Rationel Farmakoterapi 2015;(11).